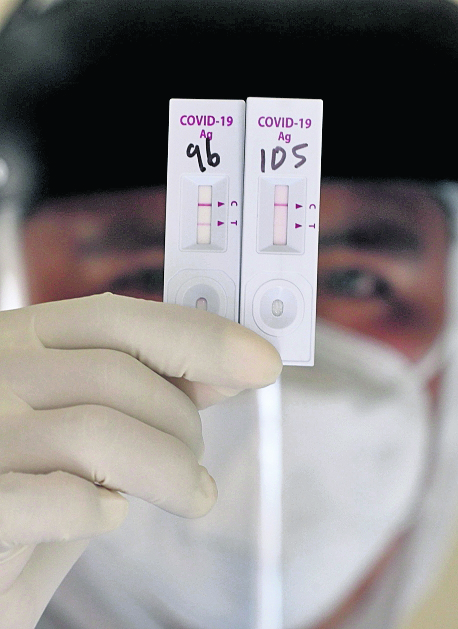
Son 82 las marcas autorizadas por el Ministerio de Salud y que disponible en el país, de estas únicamente 12 han pasado por el análisis del Laboratorio Nacional de Salud (LNS). Este no es un proceso obligatorio para los proveedores, es voluntario, pero permite conocer cómo funcionan las pruebas y cuáles pueden dar un diagnóstico preciso y confiable.
En junio del 2020 el Ministerio de Salud avaló el uso de test de antígeno para descentralizar el tamizaje y la detección de los casos de coronavirus, ya que el resultado se obtiene en pocos minutos y son fáciles de realizar, no requieren equipo especializado ni personal altamente capacitado en técnicas moleculares, contrario a las pruebas PCR, que si bien son las ideales para detectar el covid-19, solo se pueden procesar en laboratorios.
La Organización Mundial de la Salud (OMS) recomienda que las pruebas de antígeno tengan como mínimo una sensibilidad analítica mayor al 80 por ciento y una especificidad de más del 97 por ciento, pero las que fueron analizadas muestran un desempeño menor en el primer parámetro.
El LNS comparó varias marcas con el desempeño de pruebas PCR. En un primer análisis realizado en el 2020 a cuatro marcas (Biocredit, GenBody, iChroma y Standard Q) se encontró que la sensibilidad de las pruebas estaba en el rango de 52.54 y 72.62 por ciento, mientras que la especificidad estaba entre 97.6 y cien por ciento. De acuerdo con el informe de resultados del LNS, ambos parámetros mejoraron en muestras realizadas a pacientes con cargas virales elevadas.
Lea además Pruebas de antígeno podrían no detectar contagios de ómicron
Un segundo estudio se desarrolló el año pasado a otras ocho marcas. Se encontró que la sensibilidad era más baja de la indicada por el fabricante. Las pruebas examinadas fueron Anaquick COVID-19 Antígeno que reportó un 70.21 por ciento, Genedia W COVID-19 Ag obtuvo 64.63 por ciento, Human GmbH SARS-CoV-2 Ag Rapid Test alcanzó un 75.71 por ciento y Panbio COVID-19 Ag Rapid Test Device un 63.53 por ciento.
En Roche SARS-CoV-2 Rapid Antigen Test la sensibilidad fue de 74.16 por ciento, Sistema BD Veritor registro un 65.82 por ciento y Coris COVID-19 Ag Respi-Strip logró un 57.14 por ciento. El valor más bajo fue el de PCL COVID19 Ag Gold Saliva con 36.23 por ciento.
La especificidad se mantuvo alta en las ocho marcas, entre 99.11 y cien por ciento, según los resultados reportados por el LNS.
De acuerdo con el informe, el desempeño clínico de las pruebas de antígeno evaluadas cumple las recomendaciones de la OMS, a excepción de PCL COVID19 Ag Gold Saliva. Además, indica necesario continuar con la confirmación de los resultados negativos a través de una PCR.
Proceso
César Conde, jefe del LNS, menciona que al inicio de la pandemia se desconocía cómo estaban funcionando las pruebas de antígeno utilizadas por los servicios de salud, por ello, se comenzó a realizar la verificación de desempeño de las mismas.
Además, la Organización Panamericana de la Salud y la Organización Mundial de la Salud (OPS/OMS) recomiendan que dichas pruebas se sometan a una evaluación independiente para establecer su desempeño diagnóstico y examinar sus modalidades de implementación.
“Hubo una explosión de pruebas a partir de que entró el algoritmo de antígeno y no se sabía cómo estaban funcionando. Entonces, tomamos la decisión en agosto de 2020 el hacer una convocatoria pública para los proveedores que quisieran, porque es voluntario y hay tampoco hay una normativa que los obligue a venir al laboratorio a traer sus pruebas y someterlas a una comparación contra PCR y saber cómo funcionan”, dice Conde.
De esa cuenta, a la fecha 12 marcas han sido analizadas, las cuales cuentan con registro sanitario.
El procedimiento para la validación del desempeño de los test de antígeno implicó su comparación con las pruebas PCR, consideradas el estándar de oro para el diagnóstico de covid-19. En ambos casos se evaluó los parámetros de sensibilidad, la especificidad y valores predictivos.
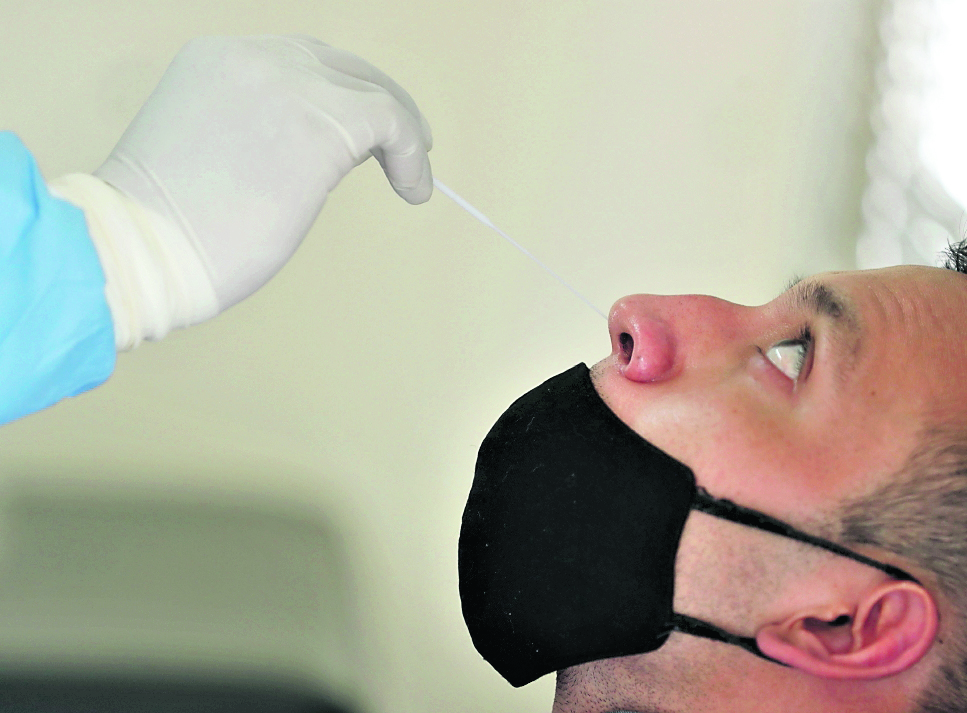
Se incluyeron muestras de casos sospechoso a covid-19 que acudieron a servicios de salud pública y al Instituto Guatemalteco de Seguridad Social. El total de muestras estudiadas fue de 2 mil 514.
En paralelo se le tomó a cada persona una muestra nasal, nasofaríngea o bien de saliva para analizar la prueba de antígeno y de PCR -protocolo Charité in house-, esta última se procesó en el LNS, adonde también se envió una copia de la ficha epidemiológica del paciente. Los dos resultados se compararon para establecer la sensibilidad, especificidad y demás valores de cada marca.
Conde indica que este paso es importante para conocer qué marcas son las que dan mejores resultados y son más fáciles de usar para los laboratorios. “Toda esa información la tenemos que indagar cómo laboratorio, porque al final nosotros también tenemos una función de orientar sobre las técnicas que son adecuadas para diagnosticar”, refiere.
Sin embargo, no hay ninguna normativa que haga obligatorio el que los proveedores sometan las pruebas de antígeno a dicha verificación.
“Aunque no esté normado, sí es obligación de LNS dar información técnica de cómo están funcionando las pruebas. Si usted como químico biólogo o laboratorista tiene una prueba con sensibilidad entre 65 y 70 por ciento y especificidad del 99 por ciento, y otra de 50 por ciento de sensibilidad, comprará la que da un mejor resultado. Nuestro objetivo principal es que la gente sepa cuál es buena y cuál no”, refiere Conde.
Otro aspecto que no está regulado es el tema de los reactivos que se utilizan en el proceso de las pruebas, para su registro basta con la documentación que presente el proveedor, no requiere de análisis de laboratorio para comprobar si funcionan o no.
En lo que respecta a Salud Pública lo más adecuado es tener una normativa que dé soporte técnico sobre el funcionamiento de las pruebas, y que no sea únicamente documental. Además, que se tenga un registro más estricto a la verificación de pruebas para detectar covid-19, así como la supervisión de los reactivos.
De acuerdo con Elena Zamora, la Junta Directiva del Colegio de Farmacéuticos y Químicos de Guatemala, se necesita tener pruebas que sean confiables y certeras para no dar resultados alejados de la realidad. “Cada país debería de hacer su propio estudio de validación porque las poblaciones son muy distintas una de otra, además, tenemos fabricantes de muchos países. Desde el punto de vista epidemiológico necesitamos saber que nos están vendiendo pruebas que funciona para Guatemala”, dice la química bióloga.
A su criterio debe normarse la verificación de las pruebas de antígeno, y además, las mesas que elaboren dicha normativa debe estar integradas por profesionales idóneos en el área.